Dalam Blog kali ini saya akan membahas tentang senyawa Natrium Bikarbonat.
Semua juga sudah tau pastinya senyawa ini apalagi kaum wanita atau ibu-ibu yang suka membuat kue. Apa itu? Ya itu adalah soda kue atau biasa disebut dengan baking soda.
Berikut penjelasan lebih rinci yang akan saya bahas.
Natrium bikarbonat adalah senyawa kimia dengan rumus NaHCO3. Dalam penyebutannya kerap disingkat menjadi bicnat. Senyawa ini termasuk kelompok garam dan telah digunakan sejak lama.
Senyawa ini disebut juga baking soda (soda kue), Sodium bikarbonat, natrium hidrogen karbonat, dan lain-lain. Senyawa ini merupakan kristal yang sering terdapat dalam bentuk serbuk. Natrium bikarbonat larut dalam air. Senyawa ini digunakan dalam roti atau kue karena bereaksi dengan bahan lain membentuk gas karbon dioksida, yang menyebabkan roti “mengembang”

Beberapa contoh yang dikenal orang sebagai berikut.
NO Nama garam Rumus Nama dagang Manfaat
1. Natrium klorida NaCI Garam dapur Penamabah rasa makanan
2. Natrium bikarbonat NaHCO3 Baking soda Pengembang kue
3. Kalsium karbonat CaCO3 kalsit Cat tembok dan bahan karet
4. Kalsium nitrat KNO3 Saltpeter Pupuk dan bahan peledak
5. Kalsium karbonat K2CO3 Potash Sabun dan kaca
6. Natrium posfat Na3PO4 TSP Deterjen
7. Amonium klorida NH4CI Salmiak Baterai kering
Diimpor dari Inggris, baking soda pertama kali digunakan di Amerika selama masa kolonial, tapi itu tidak diproduksi di Amerika Serikat sampai 1839. Pada 1846, Austin Gereja, seorang dokter Connecticut, dan John Dwight, seorang petani dari Massachusetts, didirikan sebuah pabrik di New York untuk memproduksi baking soda. Anak Dr Gereja, John, memiliki sebuah pabrik yang disebut Mills Spice Vulcan. Vulcan, dewa Romawi menempa dan api, diwakili oleh sebuah lengan dan palu, dan perusahaan kue baru soda mengadopsi logo palu dan lengan sebagai miliknya. Saat ini, Arm & Hammer merek baking soda adalah salah satu merek yang paling diakui secara luas.
Dinamakan setelah Nicolas Leblanc, kimiawan Prancis yang menciptakannya, proses Leblanc adalah sarana awal pembuatan soda abu (Na2CO 3), dari mana natrium bikarbonat dibuat. Natrium klorida dipanaskan dengan asam sulfat, memproduksi natrium sulfat dan asam klorida. Natrium sulfat kemudian dipanaskan dengan batu bara dan batu gamping untuk membentuk natrium karbonat, atau soda abu.
Pada akhir 1800-an, metode lain untuk memproduksi soda abu dirancang oleh Ernest Solvay, seorang insinyur kimia Belgia. Metode Solvay segera diadaptasi di Amerika Serikat, di mana ia menggantikan proses Leblanc. Dalam proses Solvay, karbon dioksida dan amonia diteruskan ke dalam sebuah larutan pekat natrium klorida. Natrium bikarbonat mentah presipitat keluar dan dipanaskan untuk membentuk abu soda, yang kemudian diolah dan disempurnakan lebih lanjut untuk membentuk natrium bikarbonat Amerika Serikat kemurnian Pharnacopoeia (USP).
Meskipun metode ini memproduksi baking soda abu yang digunakan secara luas, metode ini juga mempunyai masalah karena bahan kimia yang digunakan dalam proses adalah polutan dan menyebabkan masalah pembuangan.
NaHCO3 yang pertama disiapkan oleh proses Solvay, merupakan reaksi kalsium karbonat, natrium klorida, amonia, dan karbon dioksida dalam air. Ini diproduksi pada skala sekitar 100.000 ton / tahun (data 2001).
NaHCO3 dapat diperoleh dengan reaksi antara karbon dioksida dengan larutan natrium hidroksida. Reaksi awal menghasilkan natrium karbonat:
CO2 + 2 NaOH→Na2 CO3 + H2 O
Lebih lanjut penambahan karbon dioksida menghasilkan natrium bikarbonat, yang pada konsentrasi cukup tinggi akan mengendap larutan:
Na2 CO3 + CO2 + H2 O→2 NaHCO
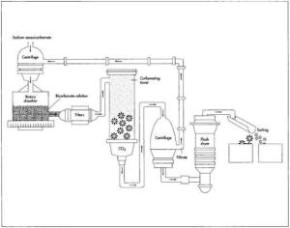
- Membuat soda abu
abu soda kimia dapat diproduksi menggunakan proses Solvay, atau dapat dibuat dari bijih Trona. Jika Trona bijih digunakan, terlebih dahulu harus ditambang. Setelah itu telah dibawa ke permukaan, bijih Trona diangkut ke berbagai pabrik pengolahan. Di sana, bijih disempurnakan menjadi bubur sesquicarbonate natrium, soda abu produk intermediate yang benar-benar berisi abu soda (natrium karbonat) dan baking soda (natrium bikarbonat).
- Selanjutnya, larutan soda abu menengah dimasukkan ke dalam centrifuge, yang memisahkan cairan dari kristal. Kristal-kristal tersebut kemudian dilarutkan dalam larutan bikarbonat (soda abu solusi yang dibuat oleh produsen) dalam dissolver putar, sehingga menjadi larutan jenuh. Solusi ini disaring untuk menghilangkan setiap bahan non larut dan kemudian dipompa melalui tangki umpan ke puncak sebuah menara carbonating.
- Karbon dioksida murni dimasukkan ke bagian bawah menara dan diproses di bawah tekanan. larutan natrium jenuh bergerak melalui menara, mendingin dan bereaksi dengan karbon dioksida untuk membentuk kristal natrium bikarbonat. Kristal ini dikumpulkan di bagian bawah menara dan ditransfer ke centrifudge, di mana solusi berlebih (filtrat) disaring. Kristal-kristal tersebut kemudian dicuci dalam larutan bikarbonat, membentuk filter cake. Sedangkan filtrat dari centrifudge didaur ulang ke dissolver rotary, di mana ia digunakan untuk kristal jenuh soda abu lebih menengah.
- Filter cake dicuci kemudian dikeringkan pada conveyor belt terus menerus atau dalam tabung pengering vertikal disebut flash dryer.
- Berikutnya, kristal kering dari natrium bikarbonat dipisahkan menurut ukuran partikel. Standar nilai natrium bikarbonat dan nilai khusus diproduksi untuk memenuhi kebutuhan spesifik pelanggan, dan ukuran partikel adalah penentu utama nilai.
Karbonat dan Bikarbonat Karbonat dan bikarbonat adalah senyawa yang melimpah dan sangat berguna serta terkenal. Kebanyakan karbonat hanya sedikit larut dalam air. Misalnya CaCO3, BaCO3, MgCO3 dan PbCO3. Banyak bikarbonat hanya stabil dalam larutan air. Contohnya ialah Ca(HCO3)2, Mg(HCO3. Semua logam IA kecuali Litium membentuk karbonat yang larut, dimana yang paling murah dan berguna adalah NaHCO3 (Soda kue), Na2CO3(Soda abu).• Karbon Disulfida(CS2) CS2 adalah cairan yang mudah terbakar dan dapat dipakai sebagai bahan pembuat CCl4,dengan reaksi:CS2 + 3Cl2 → CCl4 +S2Cl2• Hidrogen Sianida (HCN) HCN adalah senyawa gas bersifat racun,tetapi penting dalam industri seperti industri plastik.Senyawa HCN dapat dibuat secara komersil melalui reaksi:NH3 +CH4 → HCN + 3H2
Natrium bikarbonat dapat digunakan sebagai mencuci untuk menghapus apapun yang berasam.
Reaksi dari sodium bikarbonat dan asam mengahsilkang garam dan asam karbonat, yang mudah terurai menjadi karbon dioksida dan air:
NaHCO3 + HCl → NaCl + H2CO3
H2CO3 → H2O + CO2 (gas)
Reaksi dari sodium bikarbonat dan asam cuka:
NaHCO3 + CH3COOH → CH3COONa + H2O + CO2 (gas)
Natrium bikarbonat bereaksi dengan basa :
NaHCO3 + NaOH → Na2CO3 + H2O
Di atas 60°C, maka secara bertahap akan terurai menjadi sodium soda, air dan karbon dioksida. Pada suhu 200°C:
2NaHCO3 → Na2CO3 + H2O + CO2
Kebanyakan bicarbonates ini mengalami reaksi dehidrasi. Lebih lanjut Pemanasan mengubah soda menjadi oksida (sekitar 1000°C):
Na2CO3 → Na2O + CO2
Hasil reaksi penguraian NaHCO3 digunakan sebagai pemadam api.
- Berikut ini adalah karakteristik.
1. Memiliki titik lebur yang tinggi.
2. Merupakan senyawa ionik dengan ikatan kuat.
3. Dalam bentuk leburan atau larutan dapat menghantarkan listrik.
4. Sifat larutannya dapat berupa asam, basa, atau netral. Sifat ini tergantung dari jenis asam/basa kuat pembentuknya.
- KEGUNAAN
Berdasarkan sifat fisiknya,soda kue sangat bermanfaat dan digunakan untuk kehidupan rumah tangga, seperti :
- PENGHILANG BAU
Soda kue mampu menetralkan bau asam sehingga dapat digunakan sebagai penghilang bau. Anda yang mempunyai vacum cleaner, sering kali menimbulkan bau teak sedap karena kotoran yang tersimpan tidak dibersihkan dengan tuntas. Campurkan beberapa sendok soda kue kedalam kantong vacun cleaner.
Jika bau tak sedap menempel pada kain, campurkan 4 sendok makan soda kue di dalam 4 liter air. Bahkan bau tak sedap yang berasal dari sampah pun dapat dihilangkan dengan meletakkan semangkuk soda kue didalamnya.
- Pembersih
Contoh lain pemanfaatan soda kue adalah membersihkan dasar panci atau wajan yang berwarna hitam. Caranya, gosokkan soda kue dibagian yang hitam. Setelah tampak bersih , bilas bagian tersebut dengan air hingga bersih.
namun, jika ingin menghilangkan noda lemak yang menempel di permukaan perabot dapur, buatlah pasta kental dari soda kue dengan sedikit air. Gosoklah bagian yang berlemak dengan kain basah yang telah dicelupkan ke dalam pasta. Setelah digosok dengan kain basah, segera bersihkan degan menggunakan kain kering.
2. MEREDAKAN SAKIT PERUT
Manfaat soda kue ternyata tak hanya untuk perabot rumah tangga. Di bidang kesehatan, bahan dapur ini mampu membantu meredakan penyakit maag dan kembung. Caranya, larutkanlah satu sendok teh soda kue ke dalam segelas air hangat. Niscaya tubuh menjadi sehat alami. (dikutip dari kompas klasika)
3. Menetralkan asam dan basa
4. Keseimbangan pH ( kolam dan akuarium )
5. Antasid asam lambung dan mulas. Infus jika acidosis, alkalosis, kegagalan jantung, ureterosigmoidostomy, komplikasi dari hyperosmolarity metabolis
6. Masker wajah
Selain untuk rumah tangga, soda kue juga bermanfaat dalam dunia industry:
- Soda kue dapat memadamkan api sehingga dapat digunakan untuk pemadam kebakaran karena ketika dipanaskan soda kue melepaskan karbon dioksida.
- Aplikasi yang lain adalah bermanfaat dalam pengendalian pencemaran udara karena menyerap emisi sulfur dioksida dan gas asam lainnya.
Contoh Reaksi antara soda kue dengan cuka akan menghasilkan garam asetat, air dan gas karbondioksida :
NaHCO3(s) + CH3COOH(aq) → CH3COONa (aq) + H2O (l) + CO2 (gas)
Gas CO2 yang terbentuk dapat dimanfaatkan dalam berbagai proyek sains. Salah satu proyek adalah dalam pembuatan roket sederhana.
- Cara Kerja
- Alat dan Bahan
Bahan :
1) Soda kue
2) Cuka Dapur
3) Botol plastik bekas 200 mL
4) Kertas tissue
5) Sumbat botol ( harus pas dengan mulut botol )
6) Gunting, tali, dll
b. Langkah percobaan
1) Isikan cuka dalam botol plastik hingga ¼ bagian, tambahkan air sampai ½ bagian botol.
2) Siapkan sumbat botol ( ringan )
3) Bungkus 1 sendok teh soda kue dengan tissue
4) Masukkan bungkusan tissue dalam botol, kemudian segera ditutup
5) Kocok botol sebentar, kemudian diletakkan di lantai
6) Tutup botol akan terlontar
2. Teori
Persamaan Gas Ideal ( Hukum Boyle-Charles-Avogadro )
PV = nRT atau PV = m/M RT
P = tekanan ( atm )
V = volume ( liter )
n = jumlah zat ( mol )
R = konstanta gas ideal ( 0,0821 L atm mol-1 K-1 )
T = suhu ( K )
m = massa gas ( gram )
M = massa molar ( g/mol )
Rapatan Gas
m/V = MP/RT
Laju Efusi ( keluarnya gas melalui suatu lubang ) adalah volume efusi per waktu yang dibutuhkan :
v = volume efusi/waktu yang dibutuhkan
untuk gas nyata pada n mol berlaku persamaan van der Waals :
( p +n2a/v2 ) ( V – nb ) = nRT
a, b = konstanta van der waals
|
Gas
|
a
L2 atm mol-2
|
b
L mol-1
|
|
CO2
|
3,59
|
0.0427
|
|
O2
|
1,36
|
0,0318
|
Perhitungan Tekanan yang dihasilkan dari reaksi antara soda kue dengan cuka
massa NaHCO3 = 5 gram = 5g/74gmol-1 = 0,0675 mol
volume cuka = 50 mL
volume air = 50 mL
Volume ruang = 100 mL = 0,1 L
NaHCO3(s) + CH3COOH(aq) → CH3COONa (aq) + H2O (l) + CO2 (gas)
n2a = (0,0675)2 mol2.3,59 L2 atm mol-2 = 0,004556. 3,59 = 0,016356 L2 atm
nb = 0,0675 mol. 0,0427 L mol-1 = 0,00288225 L
Pada suhu kamar ( 27oC) , maka tekanan gas CO2 yang dihasilkan adalah :
P = 17,12178 – 1,6356= 15,486 atm
Jika dianggap sebagai gas ideal , maka PCO2 :
P = 16,62525 atm
Faktor lain yang perlu diperhatikan adalah massa tutup botol dan jenis bahan yang memiliki Mr-nya kecil sehingga menghasilkan tekanan gas yang lebih kuat gaya dorongnya.
D. KESIMPULAN
1. Soda Kue atau NaHCO3 bersifat amfoter agak alkalis
2. Cuka asam asetat bersifat asam lemah dan dapat bereaksi dengan garam karbonat
3. Soda Kue dan cuka bereaksi menghasilkan gas CO2 yang dapat dimanfaatkan untuk gas dorong dalam roket cuka, berdasarkan gaya tekan gas yang dihasilkan. 5 gram soda kue dan 50 mL cuka menghasilkan tekanan gas CO2 sebesar 15,486 at
http://siphemamahnyaqiral.blogspot.com/2012/04/manfaat-dari-soda-kue.html
http://dwicitranurhariyanti.wordpress.com/about-fisika/asam-basa-dan-garam/
https://www.google.co.id/search?q=NaHCO3+soda+kue&hl=jv&client=firefox-a&hs=yx2&tbo=d&rls=org.mozilla:en-US:official&source=lnms&tbm=isch&sa=X&ei=lZLEUMHqOMrsrAeA_oDAAg&ved=0CAcQ_AUoAA&biw=1024&bih=629
https://www.google.co.id/search?q=contoh+senyawa&hl=jv&client=firefox-a&hs=Ap2&tbo=u&rls=org.mozilla:en-US:official&tbm=isch&source=univ&sa=X&ei=c5DEUPHsLs3hrAeLl4GgDw&ved=0CF8QsAQ&biw=1024&bih=629
http://id.wikipedia.org/wiki/Natrium_bikarbonat
http://www.slideshare.net/luluth1/kimia-terbaru-unsurunsur-golongan-utama-2
http://slamanto.wordpress.com/2012/01/24/industri-soda-kue/
http://s2kimia.blogspot.com/2009/02/pemanfaatan-natrium-bikarbonat-soda-kue.html